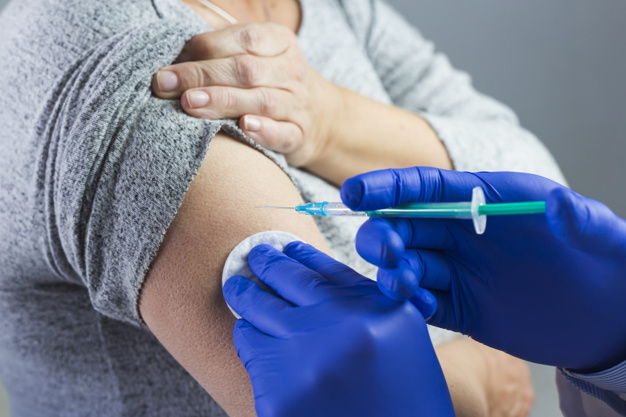
Vaccini a vettore virale: ecco cosa accomuna Astrazeneca e Johnson&Johnson
Il vaccino, come ricorda l’ISS, è un è un farmaco che induce il sistema immunitario a produrre anticorpi capaci di combattere i microrganismi responsabili di una malattia. I vaccini, e così anche quelli per il Covid-19, non sono tutti uguali, ma utilizzano tecnologie e approcci differenti per produrre nell’organismo una risposta immunitaria che impedisca lo sviluppo della malattia. Vediamo in cosa differiscono.
Sia il vaccino Vaxzevria (Astrazeneca) che Janssen (Johnson&Johnson) utilizzano come vettore virale adenovirus, ovverosia dei virus, molto comuni, responsabili del raffreddore e della faringite, che vengono inattivati, quindi sono incapaci di replicarsi e di infettare l’organismo ricevente. Poco dopo aver svolto la sua funzione, il virus vettore presente nel vaccino viene, ad ogni modo, eliminato dall’organismo.
Johnson & Johnson chiede autorizzazione a Fda per richiamo
L’azienda ha annunciato di aver inviato i dati alla statunitense Fda per ottenere l’ok alla somministrazione di un richiamo in persone dai 18 anni in su. La richiesta di integrazione all’autorizzazione all’uso di emergenza per supportare il potenziamento del vaccino a iniezione singola include i risultati dello studio di fase 3 Ensemble 2 presentati di recente, secondo i quali una seconda dose di vaccino J&J somministrata 56 giorni dopo la dose primaria ha aumentato la protezione al 94% contro la malattia sintomatica negli Stati Uniti e al 100% contro Covid grave o critica, a partire da 14 giorni dopo il richiamo.
“Siamo in contatto con l’azienda Johnson & Johnson per capire quando ci sarà un pacchetto di dati clinici che possa supportare una potenziale autorizzazione di una seconda dose del suo vaccino monodose anti-Covid. Quello che discuteremo è anche quale sia l’intervallo utile per la seconda dose. E noi potremmo decidere nelle prossime settimane cosa fare su questo”. Così Marco Cavaleri, responsabile Vaccini e Prodotti terapeutici per Covid-19 dell’Agenzia europea del farmaco Ema, spiega durante un briefing per la stampa i prossimi passi in vista per il vaccino anti-Covid J&J (sviluppato da Janssen), alla luce dei dati diffusi dall’azienda in questi giorni, non solo quelli di fase 3 su una dose booster somministrata dopo 2 mesi, ma anche quelli di fase 1/2a sul richiamo dato 6 mesi dopo la dose primaria.